
Головна сторінка Випадкова сторінка
КАТЕГОРІЇ:
АвтомобіліБіологіяБудівництвоВідпочинок і туризмГеографіяДім і садЕкологіяЕкономікаЕлектронікаІноземні мовиІнформатикаІншеІсторіяКультураЛітератураМатематикаМедицинаМеталлургіяМеханікаОсвітаОхорона праціПедагогікаПолітикаПравоПсихологіяРелігіяСоціологіяСпортФізикаФілософіяФінансиХімія
Необхідність, сутність і мета реструктуризації підприємства
Дата добавления: 2014-12-06; просмотров: 719
|
|
Воды Земли пронизывают ее, начиная с самых больших высот стратосферы вплоть до огромных глубин земной коры, достигая мантии, и образуют непрерывную оболочку планеты - гидросферу, включающую в себя всю воду в жидком, твердом, газообразном, химически и биологически связном состоянии.
Гидросфера играла и играет основополагающую роль в геологической истории Земли, в формировании физической и химической среды, климата и погоды, в возникновении жизни на нашей планете. Она развивалась вместе и в тесном взаимодействии с литосферой, атмосферой, а затем и живой природой.
Земной шар содержит около 16 млрд. км3 воды, что составляет 0,25 % массы всей нашей планеты. Из этого количества на долю гидросферы Земли (океаны, моря, озера, реки, ледники и подземные воды) приходится 1,386 млрд. км3. Пресные поверхностные воды (озера и реки) составляют всего лишь 0,2 млн. км3, а водяной пар атмосферы — 13 тыс. км3.
|
|
|
|
|
|
|
|
|
|
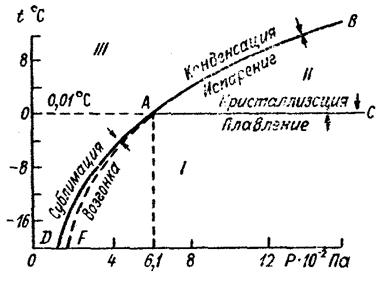
Рис. 1.1. Диаграмма агрегатных состояний воды в области тройной точки А.
I — лед. II — вода. III — водяной пар. 12*102 Па =0.012 ат
Общая масса распределенных по поверхности Земли снега и льда достигает примерно 2,5-3,0×1016т, что составляет всего лишь 0,0004% массы всей нашей планеты. Однако, такого количества достаточно, чтобы покрыть всю поверхность Земного шара 53 метровым слоем, а если бы вся эта масса вдруг растаяла, превратившись в воду, то уровень Мирового Океана поднялся бы по сравнению с нынешним примерно на 64 метра.
Вода встречается в природных условиях в трех состояниях: твердом — в виде льда и снега, жидком — в виде собственно воды, газообразном — в виде водяного пара. Эти состояния воды называют агрегатными состояниями, или же соответственно твердой, жидкой и парообразной фазами. Переход воды из одной фазы в другую обусловлен изменением ее температуры и давления. На рис. 1.1 приведена диаграмма агрегатных состояний воды в зависимости от температуры t и давления P. Из рис.1.1 видно, что в области I вода находится только в твердом виде, в области II — только в жидком, в области III — только в виде водяного пара. Вдоль кривой AC она находится в состоянии равновесия между твердой и жидкой фазами (плавление льда и кристаллизация воды); вдоль кривой AB — в состоянии равновесия между жидкой и газообразной фазами (испарение воды и конденсация пара); вдоль кривой AD — в равновесии между твердой и газообразной фазами (сублимация водяного пара и возгонка льда).
Равновесие фаз по рис.1.1 вдоль кривых AB, АС и AD надо понимать как динамическое равновесие, т. е. вдоль этих кривых число вновь образующихся молекул одной фазы строго равно числу вновь образующихся молекул другой фазы.
Если, например, постепенно охлаждать воду при любом давлении, то в пределе окажемся на кривой AC, где будет наблюдаться вода при соответствующих температуре и давлении. Если постепенно нагревать лед при различном давлении, то окажемся на той же кривой равновесия АС, но со стороны льда. Аналогично будем иметь воду и водяной пар, в зависимости от того, с какой стороны будем подходить к кривой AB.
Все три кривые агрегатного состояния — АС (кривая зависимости температуры плавления льда от давления), АВ (кривая зависимости температуры кипения воды от давления), AD (кривая зависимости давления пара твердой фазы от температуры) — пересекаются в одной точке A, носящей название тройной точки. По современным исследованиям, значения давления насыщающих паров и температуры в этой точке соответственно равны: P = 610,6 Па (или 6,1 гПа = 4,58 мм рт. ст.), t = 0,01°C (или T = 273,16 К). Кроме тройной точки, кривая АВ проходит еще через две характерные точки — точку, соответствующую кипению воды при нормальном давлении воздуха с координатами P = 1,013·105 Па и t = 100°C, и точку с координатами P = 2,211·107 Па и tкр = 374,2°C, соответствующими критической температуре — температуре, только ниже которой водяной пар можно перевести в жидкое состояние путем сжатия.
Кривые АС, АВ, AD относящиеся к процессам перехода вещества из одной фазы в другую, описываются уравнением Клапейрона—Клаузиуса:
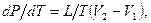
(1.1)
где T — абсолютная температура, отвечающая для каждой кривой соответственно температуре испарения, плавления, сублимации и т. д.; L — удельная теплота соответственно испарения, плавления, сублимации; V2 – V1 — разность удельных объемов соответственно при переходе от воды ко льду, от водяного пара к воде, от водяного пара ко льду. Подробное решение этого уравнения относительно давления насыщенного водяного пара e0 над поверхностью воды — кривая AB и льда—кривая AD, можно найти в курсе общей метеорологии.
Непосредственный опыт показывает, что природные воды суши при нормальном атмосферном давлении переохлаждаются (кривая AF) до некоторых отрицательных значений температуры не кристаллизуясь. Таким образом, вода обладает свойством переохлаждаться, т.е. принимать температуру ниже точки плавления льда. Переохлажденное состояние воды является состоянием метастабильным (неустойчивым), в котором начавшийся в какой-либо точке переход жидкой фазы в твердую продолжается непрерывно, пока не будет ликвидировано переохлаждение или пока не превратится в твердое тело вся жидкость. Способность воды принимать температуру ниже точки плавления льда была обнаружена впервые Фаренгейтом еще в 1724г.
Таким образом, ледовые кристаллы могут возникать только в переохлажденной воде. Переход переохлажденной воды в твердое состояние – лед, происходит только при наличии в ней центров (ядер) кристаллизации, в качестве которых могут выступать взвешенные частицы наносов, находящиеся в воде, кристаллики льда или снега, поступающие в воду из атмосферы, кристаллики льда, образующиеся в переохлажденной воде в результате ее турбулентного поступательного движения, частицы других веществ, присутствующих в водной толще.

|
| |
Рис. 1.2. Фазовая диаграмма воды.
Ih, II — IX — формы льда; 1 — 8 — тройные точки.
Переохлаждение воды – термодинамическое состояние, при котором температура воды оказывается ниже температуры ее кристаллизации. Возникает это состояние в результате понижения температуры воды или же повышения температуры ее кристаллизации. Температура воды может быть понижена отводом тепла, что наиболее часто встречается в природе, или смешением ее с соленой, например морской, водой. Температура кристаллизации может быть повышена путем понижения давления.
В лабораторных условиях при большом давлении и интенсивном охлаждении дистиллированную воду можно переохладить до температуры порядка —30, а капель —50°С. От глубины переохлаждения воды зависит и скорость ее кристаллизации.
Таким образом, диаграмму агрегатных состояний воды — сплошная линия AD на рис.1.1 — следует рассматривать как относящуюся к очень малым тепловым нагрузкам, когда влияние времени на преобразование фазы мало. При больших тепловых нагрузках процесс фазовых преобразований будет происходить согласно штриховой кривой AF.
Температура плавления льда (кривая AC) очень слабо зависит от давления. Практически кривая AC параллельна горизонтальной оси: при изменении давления от 610,6 до 1,013·105 Па температура плавления уменьшается всего лишь от 0,01 до 0°С. Однако эта температура понижается с увеличением давления только до определенного значения, затем она повышается и при очень высоком давлении достигает значения порядка 450°С (рис.1.2). Как следует из рис. 1.2, при высоком давлении лед может находиться и при положительной температуре. Насчитывают до десяти различных форм льда. Форма льда Ih, для которой характерно понижение температуры плавления с увеличением давления, соответствует обычному льду, образующемуся вследствие замерзания воды при нормальных условиях. Координаты тройных точек различных форм льда, обозначенных на рис.1.2 арабскими цифрами 1—8, приведены в табл. 1.1. Структура и физические свойства всех форм льда существенно отличаются от льда Ih.
Твердое тело (лед), как и жидкость, испаряется в широком диапазоне значений температуры и непосредственно переходит в газообразное состояние (возгонка), минуя жидкую фазу, — кривая AD. Обратный процесс, т. е. переход газообразной формы непосредственно в твердую (сублимация), осуществляется, также минуя жидкую фазу. Возгонка и сублимация льда и снега играют большую роль в природе.
| <== предыдущая лекция | | | следующая лекция ==> |
| Показники оцінки фінансового стану підприємства | | | Види реструктуризації, їх характеристика |