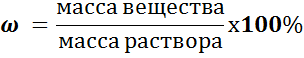Способы выражения концентрации вещества. Процентная и молярная концентрации растворов.Процентная концентрация растворов – это массовая доля растворенного вещества, которая выражается следующей математической формулой
Молярная концентрация растворов (молярность)– это чмсло молей растворенного вещества растворенного вещества в одном литре раствора, которая выражается следующей математической формулой
где, m – масса вещества; M – молярная масса вещества; V - объем раствора в мл. Если по условию дана масса раствора, то объем раствора определяют по формуле
где, V - объем раствора в мл, m – масса вещества; þ – плотность раствора (масса 1 мл раствора) Задание 3. В растворе массой 250 гр. содержится соль, массой 25 гр. Какова массовая доля соли в растворе? _____________________________________________________________________________________________________________________________________________________________________________________________ Задание 4. В 200 гр. воды растворили 50 гр. кислоты. Определить массовую долю кислоты в растворе. ___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 5. Какова масса нитрата калия, необходимого для приготовления 1 кг 20% раствора. ____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 6. В 35 гр. воды растворили 15 гр. соли. Определить массовую долю соли в растворе. ___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 7. Какой объем воды нужно взять для приготовления 120 гр. раствора с массовой долей кислоты 15%? __________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 8. К 60 гр. раствора щелочи с массовой долей 20% долили 80 мл воды. Какова массовая доля щелочи в растворе? ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 9. В 200 гр. 10% раствора соли растворили еще 25 гр. соли. Определить массовую долю соли в полученном растворе? ___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 10. 200 гр. медного купороса растворили в 800 гр. воды. Найдите массовую долю сульфата меди в образованном растворе? ______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 11. Для нейтрализации 20 гр. гидроксида натрия пошло 80 гр. нитратной кислоты. Определите массовую долю HNO3 в растворе? _____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 12. В 500 мл раствора содержится 9,8 гр H2SO4. Определите Молярность раствора. _______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 13. Сколько грамм Na2SO4 нужно взять для приготовления 200 мл двухмолярного раствора (2М Na2SO4) _______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Тема 7: Теория электролитической диссоциации
|