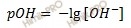Решение задачи. pOH – показатель основности раствора, pOH, равная отрицательному десятичному логарифму концентрации в растворе ионов OH−:Из соотношения:
Находим:
pOH – показатель основности раствора, pOH, равная отрицательному десятичному логарифму концентрации в растворе ионов OH−:
Используя, формулу, вычислите концентрацию ионов: pOH = 14 – 8,2 = 5,8 Отсюда: - lg [OH-] = 5,8 Вычислите концентрацию ионов: [OH-] = 10-5,8 = 0,0000016 = 1,6 ⋅ 10-6 (моль/л). Ответ: концентрацию ионов (ОН-)водного раствора равна 1,6 ⋅ 10-6 моль/л.
3. Определить константу диссоциации и pH для 0,5 нормального раствора азотной кислоты (HNO3), если степень диссоциации равна 10 %.
|