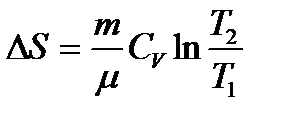Идеал газ процестерінде энтропияның өзгеруі
Барлық оқшауланған жүйеде қайтымсыз процестер өткенде жүйе энтропиясы артады. Энтропия реттелмеген, ретсіз жүйе мөлшерін көрсетеді. Энтропияның абсолют мәндерін анықтау үшін оның ең болмағанда қандай да бір белгілі температура кезіндегі абсолют мәнін білуіміз керек. Энтропияның мұндай бір мәнін Пернот ұсынған термодинамиканың ІІІ бастамасы деп аталатын теорема анықтап береді. Нерст теоремасы бойынша температура абсолют нөл болғанда қандай дененің болмасын энтропиясы нөлге тең (S = 0). Бұл қағиданы былайша түсіндіруге болады. Клаузиустың ұйғаруынша, егер бүкіл әлем кеңістігін оқшауланған жүйе деп қарастырып, оғпн термодинамиканың екінші бастамасын қолдансақ, онда оның энтропиясы бара-бара өзінің ең жоғарғы максимум мәніне жетуі керек, сөйтіп, барлық қозғалыс түрі келешекте жылуға ауысып, күллі ыстығырақ денелердің температуралары суығырақ денелерге өтіп, әлемде тепе-теңдік күй қалыптасады. Осының салдарынан әлем кеңістігіндегі барлық процестер тоқталып, жылулық апат қаупі туады деді. ХІХ ғасырда айтылған осы пікірдің бір кемшілігі термодинамиканың екінші бастамасын сол кездегі кейбір оқымыстылар (идеалистер) шегі жоқ және үздіксіз қозғалыста, дамуда болатын әлем кеңістігіне қолдануға болмайтынын түсінбеді. Кейінірек көптеген ғалымдар (материалистер) ХІХ ғасырдың аяғы мен ХХ ғасырдың басында бұл пікірді жоққа шығарды. Процестердің қайтымсыз сипаты, болуы ықтималдылығы кемірек күйден ықтималдылығы артығырақ күйге көшуімен байланысты. Демек, қайтымсыз процестердің қай бағытта жүретіндігін анықтайтын энтропия да ықтималдылықпен байланысты болуға тиісті. Больцман тұжырымдауынша, энтропия S күйдің ықтималдылығының логарифміне пропорционал болады: S = klnW Мұндағы W – берілген күйдің ықтималдылығы, ал пропорционалдық коэффициент k – Больцман тұрақтысы.
|