Химические свойства. В химическом отношении алканы – инертные вещества, что определяется прочностью связей С−С и С−НВ химическом отношении алканы – инертные вещества, что определяется прочностью связей С− С и С− Н. Кроме того, эти связи малополярны, поэтому для алканов характерны реакции, протекающие с гомолитическим разрывом связей. Для предельных углеводородов характерны два типа реакций. 1. Реакции замещения водорода с разрывом связи С− Н. В этих реакциях легче происходит замещение атома водорода, связанного с третичным углеродным атомом, труднее – со вторичным и совсем трудно – с первичным. а) Галогенирование (замещение водорода на галоген): CH4 + Cl2 хлорметан дихлорметан
CH3− CH2− CH3 + HNO3 пропан 2-нитропропан 2. Реакции расщепления молекулы алкана с разрывом связей С− Н и С− С. а) Отщепление водорода (дегидрирование алканов) с разрывом связей С− Н и образованием непредельных углеводородов: CH3− CH2− CH3 пропан пропилен б) Крекинг – расщепление молекул органических соединений под действием высоких температур с разрывом связей С− С и образованием алканов с меньшим числом атомов углерода и непредельных соединений, например: С4Н10 → СН4 + CH3− CH=CH2 или С4Н10 → С2Н6 + СН2=СН2 бутан метан пропилен бутан этан этилен
|

 CH3Cl + HCl; CH3Cl + Cl2
CH3Cl + HCl; CH3Cl + Cl2  б) Нитрование (замещение водорода на нитрогруппу) – реакция Коновалова:
б) Нитрование (замещение водорода на нитрогруппу) – реакция Коновалова: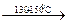 Н2О +
Н2О +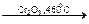 CH3− CH=CH2 + Н2
CH3− CH=CH2 + Н2


