Теоретические основы процесса сорбцииАдсорбция- это самопроизвольно протекающий диффузионный процесс, который складывается из 3-х стадий: 1 –перенос вещества из сточной воды к поверхности зерен адсорбента – внешнедиффузионная область; 2 – процесс адсорбции; 3 – перенос вещества внутри зерен адсорбента – внутридиффузионная область. Как правило, лимитирующими стадиями являются 1 и 3, однако в некоторых случаях процесс может лимитироваться сразу двумя стадиями, т.е. 1 и 3. В зависимости от характера сорбционного взаимодействия адсорбента и адсорбата различают физическую, активированную адсорбцию и хемосорбцию. Одним из критериев оценки адсорбционных свойств сорбента является изотерма адсорбции, определяющая зависимость активности адсорбента (а) от концентрации адсорбата в условиях равновесия при Т=Const: а = f(c*) Весьма важным, особенно с практической точки зрения, при адсорбционной очистке промышленных сточных вод является кинетика процесса адсорбции, т.е. скорость адсорбции, определяющая выбор технологической схемы, габариты аппаратов и другие технологические параметр. Процесс адсорбционной очистки сточных вод может осуществляться при интенсивном перемешивании адсорбента с очищаемой водой, при фильтровании сточной воды через слой адсорбента и в псевдоожиженном слое. Процесс проводится в периодическом или непрерывном режимах, в одну или несколько ступеней. Статическая одноступенчатая адсорбция на практике нашла довольно широкое применение, когда адсорбент дешев или является отходом производства. Более эффективно и при меньшем расходе адсорбента процесс протекает при использовании многоступенчатой сорбции. Расход адсорбента для одноступенчатого процесса определяется из уравнения материального баланса: M=V(Cн-Ск)/a, (1) где:m- расход адсорбента; V – расход сточной воды; Сн и Ск –начальная и конечная концентрации сточной воды; a - адcорбция. Для многоступенчатой сорбционной установки с последовательным введением сорбента в очищаемую воду расчет выполняется по формулам: Концентрация адсорбата после n-ой ступени введения сорбента Сn =(V/V+km1)n * C0 (2) В этом случае задаются дозой сорбента m1, водимой в воду на каждой ступени, и числом ступеней n m1 = V / k (n C/C0- 1) (3) Здесь задаются концентрацией адсорбата Сn после n-ой ступени и числом ступеней n. Число ступеней n =(lgC0 - lgCn) / lg(V+km1) – lgV (4) В данном случае задаются концентрацией адсорбата Cn в очищенной воде и дозой сорбента m1, вводимого на каждой ступени очистки. В формулах (2) - (4): С0- начальная концентрация сточной воды К – коэффициент распределения (к =а / С) Для исследования динамики сорбции используются выходные кривые, которые описываются экспонентой следующего вида: С = Ср exp{ln C0/Cp exp(-ατ)} (5)
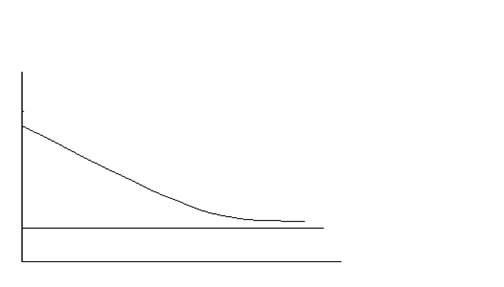
Рис.5 Кинетическая кривая Опытные точки, получаемые при снятии кинетических кривых, описываются уравнением (5). α =ln[(ln C0/Cp) / ln C/Cp]/ τ;(6) где С – любое текущее значение концентрации сточной воды. Каждой концентрации в растворе соответствует определенная концентрация в фазе сорбента:
а = (С0 – С) V / 1000 m (7)
где: V –объем раствора, мл; С0 – исходная концентрация раствора, мг/л; С – концентрация раствора к моменту времени τ,мг/л; m – масса сорбента, г; а – сорбция – мг/г.
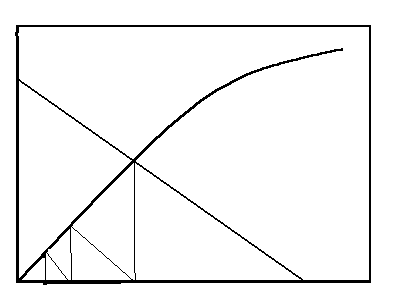
ар = (С0 – Ср) V/ 1000 m, (8) где ар – равновесная сорбция, мг/г; Ср – равновесная концентрация сточной воды, мг/л Для определения числа ступеней в многоступенчатой сорбционной установке можно использовать графический метод путем построения в координатах а =f (С) линии равновесия и рабочих линий для каждой ступени (рис.6).
С3 С2 С1 С0
Рис. 6. Определение числа ступеней в многоступенчатой сорбционной установке с последовательным введением сорбента для случая достижения равновесия на каждой ступени.
Цель работы – Исследование периодического процесса адсорбционной очистки сточных вод от органических примесей различными адсорбентами в одну или несколько ступеней при различных технологических условиях. Ход работы Для проведения процесса сорбционной очистки заданный объем модельной или реальной сточной воды, содержащей органические примеси, помещается в стакан, снабженный мешалкой с электродвигателем для перемешивания воды с адсорбентом с заданной интенсивностью путем регулирования числа оборотов мешалки. Затем в стакан добавляется заданная преподавателем навеска соответствующего сорбента, которыми могут быть, активный уголь различных марок, клиноптилолит, бентонит или др. материалы из расчета дозы 0,2 - 0,5 г на 1 л сточной воды. После добавления адсорбента включают перемешивание с заданной скоростью вращения мешалки и проводят процесс сорбции в течение 2 часов, периодически (через 15 минут) отбирая в небольшие колбочки по 5 мл пробы СВ, которые затем фильтруют через бумажный фильтр «белая» лента. Отфильтрованные пробы анализируют на содержание общего и органического углерода. По окончании анализа строят зависимость содержания общего и органического углерода (степени очистки сточных вод) от времени контакта фаз. По заданию преподавателя на той же установке может быть также рассмотрен ряд других процессов: § по изучению влияния типа адсорбента, дозы адсорбента на степень очистки воды, § выбор из различных адсорбентов наиболее эффективного при одинаковой их дозе, § по изучению влияние рН сточных вод на эффективность очистки от органических примесей, § оценка влияния интенсивности перемешивания на степень очистки воды различными адсорбентами и др. варианты
Газохроматографическое определение общего и органического углерода сточных вод (ООУ) Сущность метода анализа сточных вод на содержание общего и органического углерода заключается в хроматографическом разделении смеси из воздуха и СО2 , полученного в результате окисления пробы СВ, содержащей окисляемые органические загрязнители, с последующей индикацией процесса разделения детектором хроматографа по теплопроводности. В качестве окислителя примесей при анализе используют персульфат калия в виде насыщенного раствора, процесс окисления проводят в кислой среде при повышенном давлении и температуре на уровне 250-270 оС в специальном герметически закрываемом реакторе, схема которого приведена на рис. 1. Реактор состоит из корпуса, выполненого из нержавеющей стали, и навинчивающейся на него с помощью резьбы крышкой. Крышка имеет внутри полость, в которую через штуцера заливается вода для ее охлаждения. Для нагрева реактора используют электрическую печку с обмоткой из нихромовой проволоки. Обмотка печки сверху теплоизолирована шнуровым асбестом. Регулирование температуры в печке производится с помощью подключенного к обмотке лабораторного трансформатора. Температура измеряется с помощью ртутного термометра или термопары, присоединенной к потенциометру. Электрическая печка предварительно откалибрована по температуре путем подачи на обмотку различного напряжения. Для достижения 250 оС это напряжение составляет 50 вольт. Анализ проводится с помощью газового хроматографа марки ЛХМ-8МД, общий вид которого приведен на рис.2.
Рис. 2. Хроматограф ЛХМ-8МД 1. Блок анализатора. 2. Блок программирования. 3. Блок управления. 4. Блок подготовки газов. 5. Самопишущий прибор. 6,7- сетевые выключатели. 8. переключатель скорости нагрева в режиме программирования температуры. 9. Выключатель программатора. 10. Переключатель диапазонов. 11. Выключатель питания детектора. 12. Регулятор тока детектора. 13. Шкала милиамперметра. 14,15 Ручки установки нуля. 16. Переключатель диапазонов. 17. Регулятор температуры детектора. 18-21. Регуляторы расхода газа-носителя.22 Переключатель температуры испарителя. 23. Место ввода пробы газа на анализ. Газом-носителем является гелий, рабочая хроматографическая колонка, имеющая длину 3 м и внутренний диаметр 3 мм заполнена сорбентом «Силасорб-1» фракцией 0,25-0,50 мм. Условия детектирования: 1. Температура термостата колонок, оС - 40 2. Температура испарителя проб, оС - 225 3. Температура детектора, оС - 60 4. Ток моста детектора, мА - 100 5. Расход газа-носителя (гелия): л/час - 1,2 6. Скорость движения диаграммной ленты самописца, мм/час - 720 7. Объем вводимой пробы, мл - 1,0
|


 При τ ∞ в системе достигаются условия равновесия:
При τ ∞ в системе достигаются условия равновесия: