Теоретичний вступТема: Кінетика ферментативних реакцій типу Міхаеліса – Ментен Мета: Навчитись користуватись програмою "KINETICS" для обчислення максимальної швидкості ферментативної реакції та константи Міхаеліса. Теоретичний вступ Розглянемо реакцію взаємодії ферменту E із субстратом S з утворенням короткоживучого фермент-субстратного комплексу ES: k1 k2
k – 1 E' – вільний фермент. Загальна концентрація ферменту: [E]=[E']+[ES] [E']=[E]–[ES] (1) Кінетичне рівняння для швидкості утворення і розпаду фермент-субстратного комплексу ES:
k1 – константа швидкості перетворення E'+S→ES, k –1 – константа швидкості перетворення ES→E', k2 – константа швидкості перетворення ES→P. Після запуску ферментативної реакції деякий час концентрація фермент-субстратного комплексу ES залишається сталою (стаціонарний стан), тому k1·[E'][S]–(k –1+k2)·[ES]=0 Підставивши сюди (1), одержимо вираз для концентрації фермент-субстратного комплексу у стаціонарному стані в залежності від концентрації субстрату:
де Швидкість ферментативної реакції:
vmax=k2[E] Таким чином одержуємо рівняння Міхаеліса – Ментен:
Графік цієї залежності – лінійний – графік Лайнуївера – Берка. З графіка легко одержати величини vmax і KM.
|


 E'+S ES→E'+P
E'+S ES→E'+P
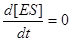 і:
і: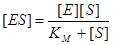
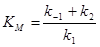 – константа Міхаеліса.
– константа Міхаеліса.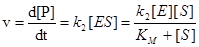
 Максимально можлива концентрація фермент-субстратного комплексу рівна концентрації ферменту: [ES]max=[E]. Отже, максимальна швидкість реакції:
Максимально можлива концентрація фермент-субстратного комплексу рівна концентрації ферменту: [ES]max=[E]. Отже, максимальна швидкість реакції: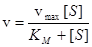
 Графічна залежність швидкості ферментативної реакції від концентрації субстрату показана на рисунку.
Графічна залежність швидкості ферментативної реакції від концентрації субстрату показана на рисунку. При малій концентрації субстрату [S] швидкість реакції
При малій концентрації субстрату [S] швидкість реакції 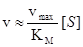 і ми маємо реакцію 1-го порядку. При високій концентрації субстрату [S] швидкість реакції прямує до максимальної: v→vmax=const і ми маємо реакцію 0-го порядку. Отже, при зростанні концентрації субстрату порядок даної реакції поступово змінюється від 1 до 0.
і ми маємо реакцію 1-го порядку. При високій концентрації субстрату [S] швидкість реакції прямує до максимальної: v→vmax=const і ми маємо реакцію 0-го порядку. Отже, при зростанні концентрації субстрату порядок даної реакції поступово змінюється від 1 до 0. З рівняння Міхаеліса – Ментен легко одержати лінійну залежність між оберненою швидкістю ферментативної реакції та оберненою концентрацією субстрату:
З рівняння Міхаеліса – Ментен легко одержати лінійну залежність між оберненою швидкістю ферментативної реакції та оберненою концентрацією субстрату:



