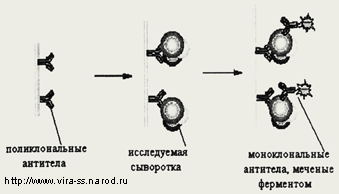
Иммуноферментный метод.Иммуноферментный метод. Объединяет возможности иммунологических и биохимических подходов. В качестве метки используются ферменты, химически сшитые с антигеном или антителом. Он шире других методов распространен в диагностической практике. Обладает высокой чувствительностью (десятые доли нанограмма на миллилитр), позволяет анализировать одновременно множество проб, может быть как качественным, так и количественным методом, легко стандартизуется, не требует большого количества времени. Существует множество различных вариантов иммуноферментного метода. Чаще всего применяется твердофазный иммуноферментный анализ (рис. 2).
Один из компонентов системы «антиген-антитело» сорбируется на твердую фазу, в качестве которой обычно используется полистирол, имеющий 96 лунок объемом 0,2 мл. В каждой лунке планшета проводится отдельная реакция, которая затем может быть отдельно проанализирована. При анализе антигенов на стенке лунок полистиролового планшета сорбируются антитела против данного антигена, затем добавляется раствор тестируемого антигена и проводится инкубация, в ходе которой происходит взаимодействие «антиген-антитело». После отмывания не-связавшегося материала в лунки планшетов добавляют антитела против того же антигена, сшитые с ферментом. Формируется связанный с твердой фазой комплекс, состоящий из антител, антигена и антител, меченых ферментом. Комплекс напоминает бутерброд, в связи с чем такой вариант иммуноферментного анализа назван сэндвич-методом. Для повышения специфичности метода используют моноклональные антитела, направленные к разным эпитопам антигена. Реакция «антиген-антитело» проявляется добавлением в отмытую лунку планшета субстрата для фермента. Используются такие субстраты, которые способны менять свою окраску в присутствии фермента. Чаще всего в качестве фермента используется пероксидаза хрена. Она расщепляет перекись водорода на воду и атомарный кислород. Последний окисляет бесцветные фенольные соединения, у которых появляется окраска. В настоящее время в этих целях применяют ортофенилендиамин (ОФД) и тетраметилбензидин (ТМБ). Появление окрашивания свидетельствует о связывании фермента с твердой фазой и, в данном случае, о положительной реакции на антиген. Количество антигена в растворе оценивается по интенсивности окрашивания раствора субстрата. Существуют конкурентные и неконкурентные методы анализа. Сэндвич-метод является неконкурентным. В конкурентном варианте определения антигена взамен антител, сшитых с ферментом, одновременно с немеченым добавляется стандартизированный антиген, меченый ферментом. Он конкурирует с немеченым антигеном за связывание с сорбированными антителами. Чем выше концентрация тестируемого (немеченого) антигена, тем меньше меченого антигена свяжется с твердой фазой. То есть в данном случае снижение интенсивности иммуноферментной реакции будет свидетельствовать о наличии антигена в тестируемом растворе. Иммуноферментный анализ применяется для определения самых различных антигенов. С его помощью тестируют наличие в крови антител к самым разным возбудителям инфекций, определяют аутоантитела, оценивают содержание вирусных и бактериальных антигенов, белков крови, опухолевых антигенов, гормонов, наркотиков и многое другое. Метод применяется не только в биомедицине и научных исследованиях, но и в сельском хозяйстве, при экологическом мониторинге и так далее. РИА. Принцип, используемый в РИА, распространяется и на другие иммунохимические и неиммунохимические методы анализа - принцип конкурентного связывания. Так, в иммуноферментном анализе (ИФА) вместо радиоактивного изотопа в качестве метки используют ферменты, а в иммунофлюориметрическом - флуоресцирующие вещества. В неиммунохимических методах роль антител выполняют реагенты, специфически связывающие определяемое вещество. Этими реагентами могут быть рецепторы гормонов или связывающие белки плазмы. В основе РИА лежит феномен конкуренции: связывание антител с антигеном, меченным радиоактивным изотопом, подавляется в присутствии немеченого антигена. Методика РИА проста и включает следующие основные этапы: К антителам добавляют меченый антиген и пробу (содержащую неизвестное количество немеченого антигена). Концентрацию антител в реакционной смеси подбирают так, чтобы число мест связывания было намного меньше общего числа антигенов. Концентрация меченого антигена должна превышать максимально возможную концентрацию антигена в пробе. Реакционную смесь инкубируют при определенной температуре заданное время. Меченный и немеченый антигены конкурентно связываются с антителами, при этом образуются иммунные комплексы, содержащие либо меченный, либо немеченый антиген. Таким образом, к концу инкубации в реакционной смеси присутствуют меченные и немеченые иммунные комплексы, а также свободные меченные и немеченые антигены. Количество меченных иммунных комплексов обратно пропорционально количеству немеченого антигена в пробе. Чтобы оценить количество образовавшихся меченных иммунных комплексов, их отделяют от оставшегося несвязанным свободного меченого антигена. Определяют концентрацию антигена в пробе по калибровочной кривой. Для ее построения используют несколько стандартных калибровочных растворов с известными концентрациями немеченого антигена. Разработано множество вариантов РИА. Методика, описанная выше, называется твердофазным РИА. Это сравнительно молодая методика. Ранее применялась более трудоемкая и долгая в постановке жидкофазная РИА (все реагенты находились в растворенном состоянии). Особая разновидность метода - иммунорадиометрический анализ (ИРМА), в котором используются меченые антитела, в отличие от РИА, где используются меченые антигены.
|