Частота столкновений и длина свободного пробега молекул
Если газ не очень плотный, то при расчете частоты столкновений следует учитывать только двухчастичные столкновения (столкновениями одновременно более чем двух молекул можно пренебречь). Задача решается в системе отсчета, связанной с рассматриваемой молекулой. Все остальные молекулы движутся с относительными скоростями и распределены по скоростям с вероятностью (98.4).
Вместо рассматриваемой молекулы можно ввести гипотетическую частицу диаметром
где n – концентрация ударяющихся молекул,
В случае однородного по составу газа формула принимает вид
где В действительности молекулы взаимодействуют не только при непосредственном соприкосновении, но и при пролете на некотором расстоянии друг от друга. Такой характер взаимодействия учитывается посредством введения эффективного сечения столкновения. Оценка для азота при нормальных условиях дает ν = 0,8 · 1010 с-1 (n = 2,7 · 1019 см –3, По средней скорости и частоте столкновений можно найти среднюю длину свободного пробега
Она зависит от плотности газа и эффективного сечения столкновения. В азоте при нормальных условиях
|

 , где
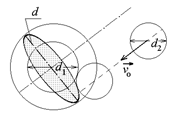
, где  – диаметры сталкивающихся молекул (рис. 42), заменив все остальные молекулы материальными точками. Таким образом, задача определения частоты столкновений сводится к нахождению числа ударов о сферу диаметром d частиц максвелловского газа:
– диаметры сталкивающихся молекул (рис. 42), заменив все остальные молекулы материальными точками. Таким образом, задача определения частоты столкновений сводится к нахождению числа ударов о сферу диаметром d частиц максвелловского газа: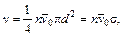 (99.1)
(99.1)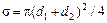 – сечение столкновения. Если газ является смесью, то рассматриваемая молекула сталкивается с молекулами различных компонент смеси. Поэтому частота всех столкновений данной молекулы равна
– сечение столкновения. Если газ является смесью, то рассматриваемая молекула сталкивается с молекулами различных компонент смеси. Поэтому частота всех столкновений данной молекулы равна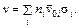 (99.2)
(99.2)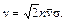 (99.3)
(99.3)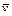 – средняя скорость теплового движения молекул,
– средняя скорость теплового движения молекул, 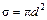 .
. = 4,5 · 104 см / с, d = 3,8
= 4,5 · 104 см / с, d = 3,8  ). Большое значение n обеспечивает ту быстроту, с которой устанавливается равновесие.
). Большое значение n обеспечивает ту быстроту, с которой устанавливается равновесие. (99.4)
(99.4)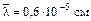 . При понижении давления
. При понижении давления  возрастает.
возрастает.


