IV. окислительные методы получения карбоновых кислотА. Окисление предельных углеводородов. Неразветвленные алканы являются одними из наиболее трудно окисляемых органических соединений. Обычные окислители не действуют на них. Лишь горячая хромовая смесь окисляет алканы с образованием большого числа продуктов, а потому практически не используется для направленного синтеза БАВ. В промышленности используется окисление твердых и жидких парафинов (С5¸С23) кислородом воздуха, чаще всего, в жидкой фазе при 100-150°С в присутствии катализаторов для получения синтетических кислот, которые являются сырьем в парфюмерии, при изготовлении смазочных веществ, моющих средств, мыла, стеарина, капрона и других полимерных материалов, а также лекарств. Суммарный выход синтетических жирных кислот составляет 60-70% в расчете на исходные углеводороды. Поскольку все метиленовые группы равноценны с точки зрения их окисляемости, получают смесь жирных кислот с цепями разной длины. В химико-фармацевтической промышленности такие процессы практически не используются. Б. Окисление активированных алкильных групп (связанных с карбонильной группой, ароматическим кольцом и другими активирующими группами) идет значительно легче и более селективно. 1. Окисление боковой цепи сложных ароматических соединений до карбоновых кислот. Для этих целей используют бихромат в кислой среде и разбавленную азотную кислоту, которые являются наиболее сильными из применяемых в химико-фармацевтической технологии окислителей. Окисление, как правило, идет по активированному a-углеродному атому. - окисление никотина разбавленной азотной кислотой:
2. Окисление толуола и его производных до бензолкарбоновых кислот так же проводят сильными окислителями (хромовой кислотой, азотной кислотой, перманганатом калия и другими). Например: - Окисление бихроматом в серной кислоте при температуре до 100°С, чем ниже температура, тем выше концентрация кислоты. - Окисление водными растворами бихромата в нейтральных растворах, но при давлении 20 МПа и температуре 305-315°С. - Окисление перманганатом калия обычно ведут постепенным добавлением твердого перманганата к водному раствору или суспензии окисляемого вещества при ~100оС.
-Окисление кислородом воздуха в присутствии катализатора (нафтената кобальта) при температуре 140°С и давлении 0,4 МПа.
Для разделения образующейся смеси продуктов реакционную массу обрабатывают раствором соды. Бензойная кислота в виде бензоата натрия переходит в водный слой и затем выделяется из него подкислением. Органический слой состоит из не вступившего в реакцию толуола и образовавшихся побочных продуктов: бензилбензоата, бензальдегида, и др.. Органический слой разделяют на составные части дистилляцией. Толуол и бензальдегид возвращают на окисление. 3. Окисление гомологов пиридина до пиридинкарбоновых кислот осуществляют: - в малотоннажных производствах, чаще всего, перманганатом по периодической схеме с выходом до 90%; - в крупнотоннажных – по непрерывной схеме азотной кислотой. Так, из пиколинов получают пиколиновую, никотиновую, изоникотиновую (a-, b-, g-пиридинкарбоновые) кислоты:
- Амид никотиновой кислоты получают также методом окислительного аминирования. Этот метод не требует дефицитного и дорогостоящего перманганата калия. Процесс можно осуществлять непрерывно:
Нитрилы пиридиновых кислот получают при пропускании смеси паров пиколина, аммиака и воздуха при 300-350°С над катализатором (на основе ванадия). Выход нитрила на прореагировавший b-пиколин 93,6%. Омыление нитрила осуществляют в водно-аммиачном растворе в присутствии едкого кали и 10%-го раствора перекиси. 4. Окисление алифатических кетонов и вторичных спиртов возможно хромовой смесью или азотной кислотой. Однако, хорошие результаты достигаются лишь в присутствии катализаторов. - Циклогексанол превращается в адипиновую кислоту под действием 50%-ой азотной кислоты в присутствии ванадата аммония с выходом 60%:
В. Окисление альдегидов в карбоновые кислоты идет очень легко. В последнее время все большее значение приобретают электрохимическиеметоды окисления альдегидов.
|


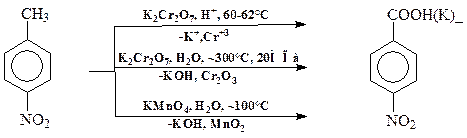

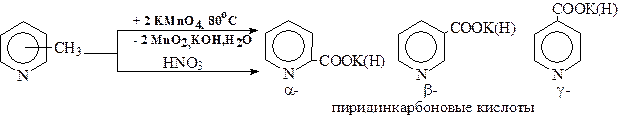 - Изоникотиновая (g-пиридинкарбоновую) кислоту является сырьем для синтеза противотуберкулезных препаратов. Никотиновая кислота (b-пиридинкарбоновая кислота) - витамин РР.
- Изоникотиновая (g-пиридинкарбоновую) кислоту является сырьем для синтеза противотуберкулезных препаратов. Никотиновая кислота (b-пиридинкарбоновая кислота) - витамин РР.




