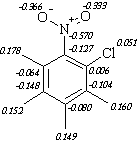
КВАНТОВО-ХИМИЧЕСКИЕ РАСЧЕТЫИспользуются две группы методов:неэмпирические - ab initio и полуэмпирические. Наиболее точные результаты дает ab initio. Оба используют SCF MO self-consistent-field molecular orbitals, то есть метод самосогласованного поля + приближения молекулярных орбиталей. Неэмпирические используют вычисление большого числа молекулярных интегралов. С увеличением размера молекулы базис расчета возрастает приблизительно пропорционально n4. Величина n – общее число базисных атомных орбиталей (АО). При учете конфигурационных взаимодействий, электронной корреляции, поправок на релятивистские эффекты и неадиабатичность существенно увеличивается время расчета. В простейшем случае неэмпирические расчеты строятся с использованием минимального базиса АО. Каждая из АО в разложении представлена одной орбиталью слейтеровского типа (STO). Минимальный базис, содержащий N гауссовских функций (GTO), примененный для аппроксимации одной слейтеровской, равняется трем – STO-3G. Вследствие больших затрат компьютерного времени на расчеты обычно используются полуэмпирические методы. Разница в том, что в полуэмпирических методах рассматриваются только взаимодействия валентных электронов, при этом некоторая часть этих интегралов параметризуется и/или задаются константами (именно это и является причиной потери точности); тогда как в ab initio все эти взаимодействия просчитываются (отсюда и большие затраты времени). Приближения, используемые в полуэмпирических методах: -CNDO =complete neglect of differential overlap (Pople, Santry, Segal/1965) рассматривает только валентные электроны. Метод аппроксимирован на атомных потенциалах и сродстве к электрону, причем некоторые из них брались как полуэмпирические величины. Первый метод назывался CNDO/1; в настоящее время используется CNDO/2, в нем улучшена параметризация. -INDO =intermediate neglect of differential overlap (Pople, Dobosh, Beveridge/1967) является улучшенным приближением CNDO, в нем пренебрегается меньшее число интегралов взаимодействия. Этот метод дает лучшие результаты, чем CNDO, особенно если важно учитывать спиновое распределение (например, в расчетах спектров электронного парамагнитного резонанса свободных радикалов). Оба метода дают достаточно хорошие результаты по геометрическим параметрам, не всегда хорошее соответствие достигается по дипольным моментам и плохие результаты по энергии диссоциации. Версии CNDO и INDO, ориентированные на расчет электронных спектров, называются CNDO/S и INDO/S. Они включают в себя учет конфигурационного взаимодействия. -NDDO =neglect of diatomic differential overlap (Pople, Santry, Segal/1965). Метод является улучшением INDO, но не дал ожидаемых результатов. Использовался до 1977 года, в котором был преобразован в MNDO. Однако все вышеперечисленные методы не давали хорошего соответствия с результатами SCF MO ab initio, поэтому была предложена целая серия методов, которая и используется на данный момент наиболее интенсивно. -MINDO/1 (Barid, Dewar/1969)-первая версия модифицированного INDO. Параметры выбирались на основе экспериментальных молекулярных теплот образования, но метод плохо воспроизводил геометрию молекулы. Поэтому в 1970 был улучшен в методе MINDO/2 (дает хорошие результаты по длинам связей и теплотам образования, но плохие по длинам связей с водородом). Следующие версии были MINDO/2’ и MINDO/3. Наиболее удачен последний, его ошибки составили 11 ккал/моль по теплоте образования, 0.02 Å по длинам связей, 5° по углам, 0.4D по дипольному моменту и 0.8 эВ по величинам потенциалов ионизации. Наибольшие ошибки проявлялись в малых циклах, соединениях с тройной связью, ароматических соединениях, компактных глобулярных молекулах и соединениях, содержащих элементы с неподеленной электронной парой. -MNDO (модифицированный MNDO) был разработан в 1977. Его ошибки по величинам: по теплоте образования 9 ккал/моль, 0.025 Å по длинам связей, 3° по углам, 0.36D по дипольному моменту и 0.5 эВ по потенциалу ионизации. -AM1 (Austin Model 1) разработан на основе MNDO в 1985 году. В нем была улучшена способность воспроизведения водородных связей, по сравнению с предшествующей версией. -PM/3 (MNDO parametric method 3; первый и второй были MNDO и AM1, соответственно) существенно снизил ошибки MNDO и AM1, при этом точность расчетов теплот образования, геометрии, дипольного момента не теряется. Если сравнивать методы MNDO, AM1, РМ3, то абсолютная ошибка по Hf298 составила 22.5%, 13.8% и 8.2% соответственно. В тонком органическом синтезе для оценки направления атаки реагента на один из альтернативных реакционных центров используют величины зарядов на них (зарядовый контроль реакции), величины и знаки коэффициентов атомной орбитали (АО) высшей занятой молекулярной орбитали или низшей свободной орбитали - АОВЗМО или АОНСМО (орбитальный контроль реакции). Для сравнения реакционной способности в ряду соединений важно знать и величины энергии граничных орбиталей ЕВЗМО и ЕНСМО. Эти данные могут быть получены с помощью квантово-химических расчетов. В реакциях электрофильного и нуклеофильного замещения в ряду ароматических и гетероароматических соединений наблюдается зарядовый контроль. На схеме приведены величины зарядов на атомах ряда молекул (расчет проведен в приближении АМ 1):
Дипольные моменты: 1,615D 5,351D ЕВЗМО = - 9,296 эВ, ЕНСМО = 0,134 эВ ЕВЗМО = - 10,314 эВ, ЕНСМО = -1,263 эВ
Экспериментально найденные величины дипольных моментов этих молекул в газовой фазе составляют соответственно 1,74D и 4,35D, что близко к расчетным данным и подтверждает корректность полученных величин. Для сравнения дипольные моменты этих молекул, найденные расчетом по методу CNDO/2, составляют - 3,151D и 6,72D. Сравнение расчетных величин дипольных моментов, полученных с помощью методов АМ 1 и CNDO/2, с экспериментальными позволяет отдать предпочтение методу АМ 1. Из величин зарядов на атомах углерода п -хлортолуола видно, что в реакциях электрофильного замещения атака электрофильного агента предпочтительнее в о- положение к метильной группе, хотя не исключается атака и в о- положение к хлору. Подробно поведение этого соединения в реакции нитрования будет рассмотрено в разделе «Реакции нитрования». В случае о- нитрохлорбезола атака электрофильного агента предпочтительнее в положение четыре ароматического цикла. Действительно при нитровании о- нитрохлорбезола в основном образуется 2,4-динитрохлорбензол. Если рассмотреть поведение этих соединений в реакциях нуклеофильного замещения, то из данных расчета видно, что при взаимодействии с нуклеофилами будет замещаться атом хлора в о- нитрохлорбезоле, а замещение хлора в п -хлортолуоле проблематично. Таким образом, в сложных случаях с помощью квантово-химических расчетов можно прогнозировать поведение молекулы в различных реакциях. Однако корректность расчетов должна быть подтверждена соответствием полученных результатов с физическими параметрами. Например, с геометрией молекулы, найденной с помощью рентгеноструктурного анализа (РСА), а в приведенных примерах с величинами дипольных моментов молекул. В противном случае из результатов квантово-химических расчетов можно сделать неправильные выводы. Квантово-химические расчеты используют также для описания механизма реакции. При этом они являются единственным не косвенным источником информации о структуре и энергетике переходных состояний, которые в принципе невозможно наблюдать экспериментально. Они также незаменимы при рассмотрении высоколабильных интермедиатов. В связи с этим экспериментальные методы не позволяют их охарактеризовать. В этих случаях ведут расчет поверхности потенциальной энергии (ППЭ).
|