Способы выражения состава раствораМассовая доля (массовый процент) растворенного вещества В – отношение массы растворенного вещества mВ к массе раствора m р-ра –
Пример: В 100 г воды растворено 82 г NaCl. Массовая доля хлорида натрия в растворе:
Молярная доля растворенного вещества В (молярный процент) – отношение количества этого вещества nВ к суммарному количеству всех веществ
Молярная концентрация (молярность) – отношение количества растворенного вещества В к объему раствора V р-ра – СМ (М), моль/л
где Пример: Молярная концентрация КOH в водном растворе, равная 1 моль/л, означает, что в 1 л такого раствора содержится 1 моль КOH Молярная концентрация эквивалента (нормальность) – отношение эквивалентного количества вещества В к объему раствора V р-ра – С н (н или N), моль экв/л
где Пример: Молярная концентрация эквивалента КOH в водном растворе, равная 1 моль/л, означает, что в 1 л раствора содержится 1 моль эквивалентного количества КOH.
Моляльная концентрация (моляльность) – отношение количества растворенного вещества В к массе растворителя Пример: Моляльная концентрация КOH в водном растворе, равная 1 моль/кг, означает, что в 1 кг воды растворен 1 моль КOH. Титр (массовая концентрация) раствора вещества В – это концентрация стандартного раствора, равная массе вещества В (
|

 – безразмерная величина (%).
– безразмерная величина (%).

 , входящих в состав раствора, включая растворитель – х – безразмерная величина (%)
, входящих в состав раствора, включая растворитель – х – безразмерная величина (%) ,
, 
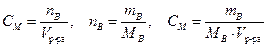 ,
, – молярная масса вещества В.
– молярная масса вещества В.
 ) = молярная масса эквивалента вещества В
) = молярная масса эквивалента вещества В , моль/кг.
, моль/кг.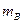 ), содержащегося в 1 см3 (мл) – ТВ, г/см3, (г/мл)
), содержащегося в 1 см3 (мл) – ТВ, г/см3, (г/мл)


