Основные газовые законыСостояние газа характеризуется его температурой, давлением и объемом. Если температура газа равна 0°С (273,15 K), а давление равно 1 атм. (1,013×105 Па = 760 мм. рт. ст.), то условия, при которых находится газ, называют нормальными. Между объемом газа и его количеством вещества существует взаимосвязь, которая описывается законом Авогадро: в равных объемах любых газов, взятых при одной и той же температуре и одинаковом давлении, содержится одинаковое число молекул. Следовательно, при одинаковых условиях 1 моль любого газа занимает один и тот же объем. Этот объем называется молярным объемом газа VM. При нормальных условиях VM = 22,4 л и число моль газа может быть вычислено по уравнению
Взаимосвязь между количеством вещества газа, его температурой, давлением и объемом устанавливает уравнение Менделеева-Клайперона:
где P – давление, Па; V – объем, м3; n – количество вещества, моль, m – масса, г; М – молярная масса газа, г/моль; R – универсальная газовая постоянная, в системе СИ R = 8,314 Дж/моль×K. На практике чаще всего приходится иметь дело со смесями газов. Каждый газ вносит свой вклад в общее давление системы – парциальное давление. Парциальным давлением называется давление, которое производил бы этот газ, занимая при тех же физических условиях объем всей газовой смеси. Парциальное давление может быть вычислено через объемное содержание газа в газовой смеси:
где Vi – объем данного газа, S Vi – общий объем газовой смеси, или через мольную долю газа:
где ni – количество вещества данного газа, S ni – сумма числа моль всех компонентов газовой смеси по уравнению:
где P – общее давление смеси газов. Общее давление смеси газов, не вступающих друг с другом в химическое взаимодействие, равно сумме парциальных давлений газов, составляющих данную смесь:
Если газ собран над жидкостью, то при расчетах его парциального давления следует иметь в виду, что оно равно разности общего давления и парциального давления пара жидкости, например, для газа, собранного над водой:
|

 .
.
 ,
,
 ,
,
 ,
,
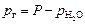 .
.



