Примеры решения задач. Определить массу и количество аммиака NH3в образце этого газа, который содержит 2,5·1025 молекул.Пример 1 Определить массу и количество аммиака NH3в образце этого газа, который содержит 2,5·1025 молекул. Решение (1 вариант) Молярная масса NH3 равна: M (NH3) = 14 + 1·3 = 17 г/моль. По закону Авогадро в 1 моле любого газа при н.у. содержится 6,02·1023 моль-1 молекул. Поэтому для нахождения массы аммиака составим и решим пропорцию: 6,02· 1023 молекул содержится в 17 г NH3; 2,5 · 1025 молекул – в X г NH3. Тогда X ( m NH3) = Количество вещества NH3 рассчитаем по формуле (2.2.2): n (NH3) = Решение (2 вариант) 1. По формуле (2.3.6) определяем количество вещества аммиака: n (NH3) = 2. Вычисляем массу аммиака: m (NH3) = n (NH3) · M (NH3) = 41,5 моль · 17 г/моль = 706 г. Пример 2 Вычислить объём, занимаемый 7 г оксида углерода (II): а) при нормальных условиях; б) при 7 0С и давлении 104,6 кПа. Решение а) Учитывая, что молярная масса СОравна 28 г/моль (М (СО) = 12 + 16 = 28 г/моль), находим объём оксида углерода при н.у., используя 1 следствие из закона Авогадро (формула 2.3.1): V 0 = б) Т.к. условия отличны от нормальных, то объем СО вычисляем, выражая его из формулы Клапейрона-Менделеева (2.3.9):
При этом параметры газа в соответствии с международной системой физических величин (СИ) выражаем: массу в кг, молярную массу – - в кг/моль, температуру – - в К, давление – - в Па:
Пример 3 Неизвестный газ имеет относительную плотность по воздуху 1,31. Определить массу образца этого газа объемом 68 л (объем приведен к нормальным условиям).
|

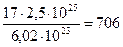 г.
г.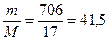 моль.
моль.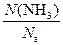 =
= 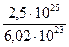 = 41,5 моль.
= 41,5 моль.  л.
л.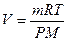 .
. м3.
м3.


