ПОЛЯРИЗАЦИЯПоляризация – взаимное смещение ядра и электронной оболочки внешнего электронного слоя под действием электрического поля соседнего иона. Поляризуемость – степень деформации иона при поляризации. Поляризующая способность – способность иона оказывать поляризующее воздействие. В химических соединениях с полярной ковалентной и ионной связью наблюдаются явления взаимной поляризации катионов и анионов (двусторонняя поляризация) или преимущественной поляризации одного из ионизированных атомов (односторонняя поляризация). Поляризационные эффекты зависят от электронной структуры ионизированных атомов, от их радиуса и эффективного или реального заряда. Различают поляризуемость и поляризующие действия условных и реальных катионов и анионов (табл.2.1) Таблица 2.1
Следует учитывать отличие электронной структуры реальных и условных катионов и анионов от структуры соответствующих атомов элементов. Электронные структуры внешнего квантового слоя катионов различных s – p – d – f элементов изменяются в соответствии со степенью окисления атомов (+ о.ч.) Образование катионов s-элементов сопровождается потерей s-электронов с внешнего квантового слоя, если окислительное число (+о.ч.) не достигает максимального значения, определяемого номером группы в периодической системе Д.И. Менделеева. При удалении всех валентных s- и p-электронов роль внешнего квантового слоя начинает играть предвнешний квантовый слой. Для катионов d- и f-элементов характерна потеря двух (одного) s-электронов с внешнего квантового слоя. В зависимости от значения (+о.ч.) в процессе ионизации d-элементы теряют также d-электроны с предвнешнего квантового слоя, а f-элементы способны отдавать, кроме того, f-электроны с предвнешнего квантового слоя. Таким образом, во всех случаях, когда внешним квантовым слоем у катионов s – p – d – f-элементов становится их предвнешний квантовый слой, электронная структура его может изменяться в пределах от 8-электронной (s p) до 18-электронной (s p d). Исключение составляют катионы s и p-элементов второго периода, у которых после потери всех валентных электронов предвнешний квантовый слой имей 2-электронную структуру. Для иллюстрации указанных закономерностей сопоставим электронные формулы атомов и катионов различных химических элементов (табл.2.2). Таблица 2.2
Катионы, обладающие одинаковой электронной структурой, называют изоэлектронными. Очевидно, что радиусы катионов всегда меньше радиусов соответствующих атомов за счет потери электронов и уменьшаются по мере увеличения окислительного числа (+о.ч.) (см таблицу 5.1). Для элементарных анионов характерны электронные структуры внешнего квантового слоя типа 8-электронной оболочки, поскольку при формировании анионов атомы элементов неметаллов принимают электроны, обычно дополняя структуру внешнего квантового слоя до 8-электронной. Сопоставим электронные структуры некоторых атомов элементов неметаллов и соответствующих анионов (табл.2.3). Таблица 2.3
Анионы, обладающие одинаковой электронной структурой, называют изоэлектронными. Очевидно, что радиусы анионов больше радиусов соответствующих атомов элементов за счет присоединения электронов (см. таблицу 5.1).
|

 / 3s²3p¹
Sn 1s² / 2s²2p
/ 3s²3p¹
Sn 1s² / 2s²2p  / 3s²3p
/ 3s²3p 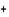 ¹ 1s²
Al
¹ 1s²
Al  1s² / 2s²2p
1s² / 2s²2p  1s² / 2s²2p
1s² / 2s²2p 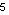
 ³ 1s² / 2s²2p³2p
³ 1s² / 2s²2p³2p  ¹ 1s² / 2s²2p
¹ 1s² / 2s²2p 


