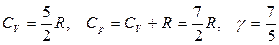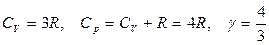Измерение и обработка результатов1. Налить в кипятильник воды столько, чтобы уровень ее был ниже верхнего края кипятильника на 3 – 4 см. 2. Включить нагреватель D в сеть. 3. Через 5 мин. после начала кипения воды в кипятильнике налить в калориметр мензуркой 200 см3 холодной водопроводной воды. Перемешав воду в калориметре мешалкой, замерить ее температуру Т 1. Этот момент считать началом опыта. Поставить калориметр на подставку, которую поднять так, чтобы пластинка покрылась водой на 3 – 4 мм. Начать отсчет времени по часам. 4. Когда температура воды в калориметре повысится на 8 – 10oС, прекратить отсчет времени и записать конечную температуру Т 2. В процессе нагревания воду в калориметре перемешивать, быстро поднимая и опуская калориметр. 5. Слить нагретую воду, промыть калориметр и, влив снова 200 см3 воды, повторить опыт еще два раза. По окончании опыта выключить нагреватель D. ПРИМЕЧАНИЕ: вода в кипятильнике должна кипеть до конца измерений, чтобы температура Т 3была постоянной. 6. Результаты опытов занести в журнал наблюдений. Журнал наблюдений
(l = 0.14 м – длина стержня; D = 0.017 м – диаметр стержня; CΣ = 894 Дж/К). Контрольные вопросы: 1. Что называется количеством теплоты? Единица его измерения? 2. Что называется явлением теплопроводности? 3. 3.Теплопроводность относится к явлениям переноса. Перенос какой физической величины происходит в этом случае? Приведите примеры других явлений переноса. 4. Объясните явление теплопроводности с точки зрения молекулярно-кинетической теории. 5. Какое состояние потока тепловой энергии называется стационарным? 6. Каким законом описывается явление теплопроводности? Напишите формулу этого закона и объясните смысл физических величин, входящих в него. 7. Какой физический смысл имеет коэффициент теплопроводности? От чего зависит коэффициент теплопроводности? 8. Опишите устройство калориметра. Литература 1. Савельев И.В. Курс общей физики: В 3-х т. М.: Наука, 1982. Т.1. 2. Сивухин Д.В. Общий курс физики: Молекулярная физика и термодинамика. М.: 1981. Т.2. 3. Трофимова Т.И. Курс физики. М.: Высш. Школа, 1985. 4. Яворский Б.М., Детлаф А.А. Справочник по физике. М.: Наука, 1985.
Лабораторная работа № 11(21) Определение отношения теплоемкостей газа Выполнил студент _______________, группа __________, дата ____________. Допуск ______________ Выполнение __________ Зачет ________________
Цель работы: Найти величину отношения CP /CV для воздуха. Приборы и материалы
Теоретические сведения Основные понятия и законы Теплоёмкость Теплоёмкость тела (обычно обозначается латинской буквой C) — физическая величина, определяющая отношение бесконечно малого количества теплоты δQ, полученного телом, к соответствующему приращению его температуры δT:
Единица измерения теплоёмкости в СИ — Дж/К. Теплоемкость тела зависит только от его химического состава, массы, вида термодинамического процесса, в широком интервале температур – от температуры. Понятие теплоёмкости определено как для веществ в различных агрегатных состояниях (твёрдых тел, жидкостей, газов), так и для ансамблей частиц и квазичастиц (в физике металлов, например, говорят о теплоёмкости электронного газа). Удельная и молярная теплоёмкости Удельной теплоемкостью вещества называется физическая величина, численно равная количеству энергии в форме теплоты, которое надо сообщить единице массы этого вещества для увеличения его температуры на 1 Кельвин (т.е. это теплоёмкость, отнесённая к единице массы вещества):
В общем случае удельная теплоемкость зависит от рода вещества и от вида термодинамического процесса, в котором телу сообщается количество теплоты. Удельные теплоёмкости многих веществ приведены в справочниках (обычно для процесса при постоянном давлении). К примеру, удельная теплоёмкость жидкой воды при нормальных условиях — 4200 Дж/(кг·К); Количество теплоты, поглощённой телом при изменении его состояния, зависит не только от начального и конечного состояний (в частности, от их температуры), но и от способа, которым был осуществлен процесс перехода между ними. Поэтому для газов различают два вида теплоемкостей: если газ нагревают, сохраняя его объем постоянным (изохорно), говорят об удельной теплоемкости газа при постоянном объеме c V; если же газ нагревают, сохраняя постоянным его давление (изобарно), то говорят об удельной теплоемкости газа при постоянном давлении с Р. У жидкостей и твёрдых тел разница между Ср и Cv сравнительно мала. Часто пользуются молярной теплоемкостью Сμ, которая, в отличие от удельной теплоемкости, отнесена не к единице массы (1 килограмму), а к массе одного моля вещества. Очевидно, что Cμ = m c, Дж/(моль×К) Для газов молярную теплоемкость, рассчитанную при постоянном давлении, обозначают С Р, а рассчитанную при постоянном объеме – С V. Следовательно, С Р = m× c P, C V = m× c V. Когда нагревание газа происходит при постоянном объеме, газ не совершает механической работы и все сообщаемое газу тепло идет только на увеличение его внутренней энергии D U, т.е.: D Q = m × c V×D T = D U. Если же нагревание газа происходит при постоянном давлении и, следовательно, объем газа увеличивается, то сообщаемое газу тепло D Q идет как на увеличение его внутренней энергии D U, так и на совершение газом работы D A над внешними телами, т.е. D Q = m × c P×D T = D U + D A. Из сопоставления формул следует, что c P > c V, т.е. удельная теплоемкость газа при постоянном давлении больше удельной теплоемкости того же газа при постоянном объеме. При этом, согласно уравнению Майера: C P = C V + R. В данной работе требуется определить не абсолютные значения теплоемкостей газа, а их отношение, называемое коэффициентом Пуассона:
Теоретическое вычисление теплоемкости, в частности её зависимости от температуры тела, не может быть осуществлено с помощью чисто термодинамических методов и требует применения методов статистической физики. Теплоёмкость идеального газа Для газов вычисление теплоемкости сводится к вычислению средней энергии теплового движения отдельных молекул. Это движение складывается из поступательного и вращательного движений молекулы как целого и из колебаний атомов внутри молекулы.
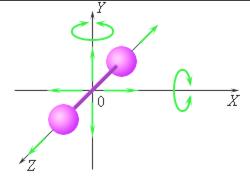
На рис.1 изображена модель двухатомной молекулы. Молекула может совершать пять независимых движений: три поступательных движения вдоль осей X, Y, Z и два вращения относительно осей X и Y. Опыт показывает, что вращение относительно оси Z, на которой лежат центры обоих атомов, может быть возбуждено только при очень высоких температурах. При обычных температурах вращение около оси Z не происходит, так же как не вращается одноатомная молекула. Каждое независимое движение называется степенью свободы. Таким образом, одноатомная молекула имеет 3 поступательные степени свободы, «жесткая» двухатомная молекула имеет 5 степеней (3 поступательные и 2 вращательные), а многоатомная молекула – 6 степеней свободы (3 поступательные и 3 вращательные). В классической статистической физике доказывается так называемая теорема о равномерном распределении энергии по степеням свободы: если система молекул находится в тепловом равновесии при температуре T, то средняя кинетическая энергия равномерно распределена между всеми степенями свободы и для каждой степени свободы молекулы она равна 1\2 kT, где k = 1,38×10- 23 Дж/К – постоянная Больцмана. Из этой теоремы следует, что молярные теплоемкости газа C p и C V и их отношение γ могут быть записаны в виде
где i – число степеней свободы молекулы газа. Для газа, состоящего из одноатомных молекул (i = 3):
Для газа, состоящего из двухатомных молекул (i = 5):
Для газа, состоящего из многоатомных молекул (i = 6):
Экспериментально измеренные теплоемкости многих газов при обычных условиях достаточно хорошо согласуются с приведенными выражениями. Однако, в целом классическая теория теплоемкости газов не может считаться вполне удовлетворительной. Существует много примеров значительных расхождений между теорией и экспериментом. Это объясняется тем, что классическая теория не в состоянии полностью учесть энергию, связанную с внутренними движениями в молекуле. Теорему о равномерном распределении энергии по степеням свободы можно применить и к тепловому движению частиц в твердом теле.
|

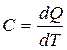
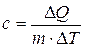 , Дж/(кг×К)
, Дж/(кг×К)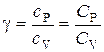 .
.