Будова молекули МетануЕлектронна будова атома вуглецю: 1s22s22p2 6С збуджений стан
При " змішуванні" чотирьох орбіталей збудженого атома вуглецю (однієї 2s- і трьох 2p- орбіталей) утворюються чотири рівноцінні sp3- гібридні орбіталі.
Рис.1. Схема електронної будови молекули метану
Рис.2. Утворення молекули етану за рахунок перекривання двох гібридних електронних хмар атомів вуглецю.
12.1.3. Ізомерія Перші алкани в гомологічному ряді – метан, етан, пропан – не мають ізомерів. Четвертий – бутан C4H10 має два ізомери: ● з нерозгалуженим вуглецевим ланцюгом
● з розгалуженим ланцюгом
Ізомерія, при якій речовини відрізняються одна від одної порядком зв'язку атомів в молекулі, називається СТРУКТУРНОЮ або ізомерією вуглецевого скелету.
|

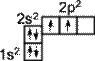 ––† 6С*
––† 6С* 
 sp3- ГІБРИДИЗАЦІЯ характерна для атомів вуглецю в насичених вуглеводнях (алканах) – зокрема, в метані.
sp3- ГІБРИДИЗАЦІЯ характерна для атомів вуглецю в насичених вуглеводнях (алканах) – зокрема, в метані.
 (нормальний бутан)
(нормальний бутан) Ізобутан (2-метил-пропан)
Ізобутан (2-метил-пропан)


