Гомогенные химические реакцииСкорость гомогенной химической реакции равна изменению концентрации какого-либо из веществ, вступающих в реакцию или образующихся в результате ее, в единицу времени. Зависимости концентраций исходных веществ или продуктов реакции от времени называются кинетическими кривыми (рис. 4.1). В ходе реакции количества исходных веществ во времени убывают, количества продуктов реакции увеличиваются. Скорость является положительной величиной, поэтому перед отношением в правой части уравнения ставят знак «минус», если ее определяют по расходу исходного вещества, и знак «плюс», если ее определяют по увеличению концентрации продукта реакции. В общем случае
Отношение изменения концентрации одного из реагирующих веществ к промежутку времени выражает среднюю скорость реакции
Из определения скорости и анализа уравнения (4.1) следует, что скорость реакции имеет единицу измерения [моль∙л-1·с-1] (иногда [моль∙м-3·с-1], [моль·л-1·ч-1] и т.п.).
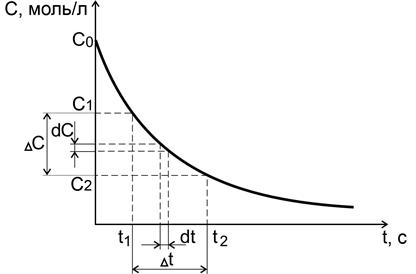
Рис. 4.1. Средняя и истинная скорости реакции для исходного вещества В ходе реакции изменяются концентрации реагирующих веществ и соответственно скорость реакции. Средняя скорость реакции тем ближе к истинной скорости, чем меньше промежуток времени D t. За бесконечно малый промежуток времени dt концентрация изменится на бесконечно малое значение dC. Скорость реакции в данный момент времени, или мгновенная (истинная) скорость реакции, представляет собой первую производную концентрации реагирующего вещества по времени
При описании кинетического процесса необходимо указывать вещество, по отношению к которому была измерена скорость («скорость по веществу»). Рассмотрим в качестве примера следующую реакцию: N2 + 3H2 = 2NH3. Из уравнения реакции видно, что если за какой-то период времени D t в реакцию вступит n молей N2, то за это же время прореагирует 3 n молей Н2 и образуется 2 n молей NH3. Следовательно, скорости реакции по каждому из веществ различны, однако, разделив эти скорости на стехиометрический коэффициент, соответствующий этому веществу в уравнении реакции, получим одну и ту же величину – просто «скорость реакции»
|

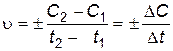 .
.
 .
.
 .
.
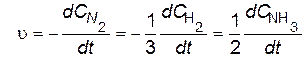 .
.


