Хід роботи. 1. Зважте внутрішню склянку калориметра.1. Зважте внутрішню склянку калориметра. 2. Відміряйте циліндром 50 мл розчину натрій гідроксиду (NaOH), внесіть його в склянку і визначте температуру. 3. Відміряйте циліндром 50 мл розчину хлоридної кислоти (HCl). 4. Термометр опустіть у розчин хлоридної кислотиі визначте температуру. 5. Розчин кислоти вилийте в розчин лугу і простежте за зміною температури. Запишіть кінцеву максимальну температуру розчину. 6. Отримані дані занесіть у таблицю 2.1.
Таблиця 2.1
7. Виконайте розрахунки: 7.1. Теплоти, що виділяється чи поглинається в калориметрі, за формулою: Q = (mp · Cp + mск · Сск) · DT, де mp – маса розчину, г; Cp – питома теплоємність розчину дорівнює питомій теплоємності води, тобто 4,184 Дж/(г·К); mск – маса склянки, г; Сскла – питома теплоємність скла дорівнює 0,753 Дж/(г·К). Q = ___________________________________________________________________ 7.2. Кількості моль-еквівалентів кислоти, що приймає участь в реакції. ____________________________________________________________________________________________________________________________________________ 7.3. Теплоти нейтралізації ( ____________________________________________________________________________________________________________________________________________ 7.4. Теплового ефекту ____________________________________________________________________________________________________________________________________________ 8. Визначте відносну похибку досліду за формулою:
9. Висновок _______________________________________________________________________________________________________________________________
Завдання для самоконтролю до теми "Хімічна термодинаміка";
1. Що вивчає термохімія? 2. Дайте визначення тепловому ефекту реакції. Назвіть типи хімічних реакцій за тепловим ефектом? 3. Сформулюйте закон Гесса та його наслідки. 4. Які рівняння називаються термохімічними? 5. Як визначити тепловий ефект реакції за стандартними ентальпіями утворення та стандартними ентальпіями згоряння? 6. Від чого залежить тепловий ефект реакції? 7. Які параметри стандартного стану? 8. Що характеризує ентропія? 9. За значенням якої термодинамічної функції можна визначити напрямок перебігу процесу для ізольованих та неізольованих систем? 10.Порівняйте а) Fe2O3(к) + 3CO(г) = 2Fe(к) + 3CO2(г); б) Fe2O3(к) + 3C(графіт) = 2Fe(к) + 3CO(г); в) Fe2O3(к) + 3Н2(г) = 2Fe(к) + 3Н2O(г). 11. Обчисліть значення а) Cu(к) + ZnO(к) = CuO(к) + Zn(к); б) FeO(к) + CO(г) = Fe(к) + CO2(г); в) 3Fe3O4(к)+ 8Al(к)= 9Fe(к) + 4Al2O3(к); г) FeO(к) + 1/2C(графіт) = Fe(к) + 1/2CO2(г). 12. Обчисліть значення 13. Визначте знак зміни ентропії а) 2NO(г) + O2(г) = 2NO2(г); б) 2H2S(г) + 3O2(г) = 2H2O(p) + 2SO2(г); в) CO2(к) = CO2(г); г) 2N2(г) + O2(г) = 2N2O(г); д) NH4NO3(к) =N2(г) + 2H2O(г) + ½O2(г).
|

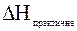 ) для 1 моль еквівалента кислоти.
) для 1 моль еквівалента кислоти.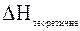 реакції нейтралізації одного еквівалента сильної кислоти (чи лугу) за скороченим йонним рівнянням: Н+(р) + ОН–(р) = Н2О(р), якщо
реакції нейтралізації одного еквівалента сильної кислоти (чи лугу) за скороченим йонним рівнянням: Н+(р) + ОН–(р) = Н2О(р), якщо 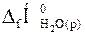 =–286,0 кДж/моль;
=–286,0 кДж/моль; 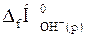 =–230,2 кДж/моль;
=–230,2 кДж/моль;  = 0.
= 0. ._____________________________________________
._____________________________________________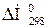 реакцій відновлення ферум (ІІІ) оксиду різними відновниками при 298 К та визначте, якою із речовин можна найбільш ефективно і повно відновити залізо із оксиду Fe2O3 за умови 1100 К.
реакцій відновлення ферум (ІІІ) оксиду різними відновниками при 298 К та визначте, якою із речовин можна найбільш ефективно і повно відновити залізо із оксиду Fe2O3 за умови 1100 К. реакцій та визначте, які з них можливі:
реакцій та визначте, які з них можливі: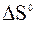 наступних процесів за рівняннями:
наступних процесів за рівняннями:


