Стандартные электродные потенциалы (Е°) при 25°С
| Элемент
| Полуреакция
| Eo,В
| |
|
|
| | Ag
| Ag+ + e = Ag↓
| +0,7994
| | AgBr↓ + e = Ag↓ + Br–
| +0,071
| | AgCl↓ + e = Ag↓ + Cl–
| +0,222
| | AgI↓ + e = Ag↓ + I–
| –0,152
| | As
| H3AsO4 + 2H+ + 2 е = HAsO2 + 2H2O
| +0,56
| 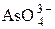 + 2H2O + 2 е = + 2H2O + 2 е =  + 4ОН– + 4ОН–
| –0,71
| | Br
| Br2 + 2 e = 2Br–
| +1,087
| 2 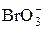 + 12H+ + 10 e = Br2↓ + 6H2O + 12H+ + 10 e = Br2↓ + 6H2O
| +1,52
| 2 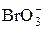 +6H2O + 10 e = Br2↓ + 12OH– +6H2O + 10 e = Br2↓ + 12OH–
| +0,50
| | C
| CO2↑ + 2H+ + 2 e = HCOOH
| –0,20
| | 2CO2↑ + 2H+ + 2 e = H2C2O4
| –0,49
| | Са
| Са2+ + 2 e = Ca↓
| –2,79
| | Cd
| Cd2+ + 2 e = Cd↓
| –0,403
| | Се
| Се4+ + e = Ce3+
| +1,77
| | Сl
| Сl2↑ + 2 e = 2C1–
| +1,359
| | 2HOС1 + 2Н+ + 2 e = Cl2↑+H20
| +1,63
| | 2C1O–+2H2O + 2 e = С12↑ +4OH–
| +0,40
| | HC1O + H+ + 2 e = Сl– + Н2О
| +1,50
| Продолжение табл. 14
|
|
|
| | Cl
| ClO– + H2O + 2 e = Сl– + 2OН–
| +0,88
| | НСlO2+2H+ + 2 e = HClO + H2O
| +1,64
| | 2HClO2 + 6H+ + 6 e = Cl2↑+4H2O
| +1,63
| | HClO2 + 3H+ + 4 e = Cl– + 2H2O
| + 1,56
| 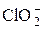 + H2O + 2 e = ClO– + 2OН– + H2O + 2 e = ClO– + 2OН–
| +0,66
| 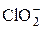 + 2H2О + 4e = C1– + 4OH– + 2H2О + 4e = C1– + 4OH–
| +0,77
|  +3Н+ + 2 e = HC1O2 + H2O +3Н+ + 2 e = HC1O2 + H2O
| +1,21
|  + H2O + 2e = + H2O + 2e = 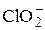 + 2OH– + 2OH–
| +0,33
|  + 2H+ +e = C1O2↑ + H2O + 2H+ +e = C1O2↑ + H2O
| +1,15
|  + 6H+ +6 e = Cl– + 3H2O + 6H+ +6 e = Cl– + 3H2O
| +1,45
|  + 3H2O+6 e = Сl– + 6OН– + 3H2O+6 e = Сl– + 6OН–
| +0,63
|  + 2H+ + 2 e = + 2H+ + 2 e =  + Н2О + Н2О
| +1,19
|  +H2O+2 e = +H2O+2 e =  + 2OH– + 2OH–
| +0,36
| 2  + 16H++ 14 e = С12↑ +8Н2О + 16H++ 14 e = С12↑ +8Н2О
| +1,39
|  + 8H+ + 8 e = Сl– + 4Н2О + 8H+ + 8 e = Сl– + 4Н2О
| +1,38
|  + 4H2O + 8 e = С1– + 8OН– + 4H2O + 8 e = С1– + 8OН–
| +0,56
| | Со
| Со3+ + e = Со2+
| +1,95
| | Со2+ + 2 e = Со↓
| –0,29
| 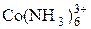 + e = + e = 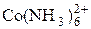
| +0,1
| | Cr
| Cr3+ + e = Сr2+
| –0,41
| | Сr3+ + 3 e = Сr↓
| –0,74
| 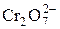 + 14Н+ + 6 e = 2Сr3+ + 7Н2О + 14Н+ + 6 e = 2Сr3+ + 7Н2О
| +1,33
| 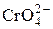 + 4Н2О + 3 e = Сr(ОН)3↓+5ОН– + 4Н2О + 3 e = Сr(ОН)3↓+5ОН–
| –0,13
| | Сu
| Cu2+ + 2 e = Сu↓
| +0,345
| | Cu+ + e = Сu↓
| +0,531
| Продолжение табл. 14
|
|
|
| | Сu
| Cu2+ + e = Сu+
| +0,159
| | F
| F2↑ + 2 е = 2F–
| +2,77
| | Fe
| Fe3+ + е = Fe2+
| +0,771
| | Fe3+ + 3 e = Fe↓
| – 0,058
| | Fe2+ + 2 е = Fe↓
| – 0,473
| 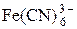 + e = + e = 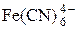
| +0,364
| | Ga
| Ga3+ + 3 e = Ga↓
| – 0,56
| | H
| 2H+ + 2 е =H2↑
| 0,0000
| | 2H2O + 2 е = H2↑ +2OH–
| –0,828
| | H2O2 + 2H+ + 2 е = 2H2O
| +1,77
| 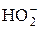 + H2O + 2 e = 3ОH– + H2O + 2 e = 3ОH–
| +0,88
| | Hg
| 2Hg2+ + 2 е = 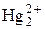
| +0,907
| | Hg2+ + 2 е = Hg↓
| +0,850
| 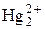 + 2 е = Hg↓ + 2 е = Hg↓
| +0,792
| | I
| I2↓ + 2 е = 2I–
| +0,536
| | I2 + 2 е = 2I–
| +0,621
|  + 2 е =3I– + 2 е =3I–
| +0,545
| | 2IBr + 2 е = I2↓ + 2Br–
| +1,02
| | ICN↑ + 2 е = I– + CN–
| +0,30
| | 2ICN↑ + 2H+ + 2 е =I2↓ +2HCN
| +0,63
| | 2ICl↑ + 2 е = I2↓ + 2Cl–
| +1,19
| | 2НIО + 2Н+ + 2 е = I2↓+2H2O
| +1,45
| | 2IO– + H2O + 2 е = I2↓ + 4OH–
| +0,45
| | HIO + H+ + 2 е = I– + H2O
| +0,99
| | IO– + H2O+2 е = I– + 2OH–
| +0,49
| Продолжение табл. 14
|
|
|
| |
| 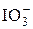 + 5H++ 4 е = HIO + 2H2O + 5H++ 4 е = HIO + 2H2O
| +1,14
| 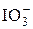 +2H2O + 4 е = IO– + 4OH– +2H2O + 4 е = IO– + 4OH–
| +0,14
| 2 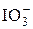 + 12H+ + 10 e = I2↓ + 6H2O + 12H+ + 10 e = I2↓ + 6H2O
| +1,19
| 2 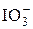 +6H2O + 10 e = I2↓ + 12OH– +6H2O + 10 e = I2↓ + 12OH–
| +0,21
| 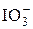 + 6H+ + 6 е = I– + 3H2O + 6H+ + 6 е = I– + 3H2O
| +1,08
| 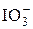 + 3H2O + 6 е = I– + 6OH– + 3H2O + 6 е = I– + 6OH–
| +0,26
| H5IO6 + H+ + 2 е = 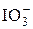 + 3H2O + 3H2O
| ≈+1,6
| 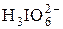 + 2 е = + 2 е = 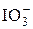 + 3OН– + 3OН–
| ≈+0,7
| | H5IO6 + 7H+ + 8 е = I– + 6Н2О
| ≈+1,24
| 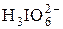 + 3H2O + 8е = I– + 9OН– + 3H2O + 8е = I– + 9OН–
| ≈+0,37
| | In
| In3+ + 3 е =In↓
| –0,34
| | Ir
| Ir3+ + 3 е = Ir↓
| ≈+1,15
| | К
| K++ e = К↓
| –2,923
| | La
| La3+ + 3 е = La↓
| –2,52
| | Li
| Li+ + е = Li↓
| –3,04
| | Mg
| Mg2+ + 2 е = Mg↓
| –2,37
| | Мn
| Мn3+ + е = Мn2+
| +1,51
| | Мn2+ + 2е = Мn↓
| –1,17
| | Mn(OH)3↓ + e = Мn(ОН)2↓ + OH–
| +0,1
| | MnO2↓ + 4H+ + 2 е = Мn2++2Н2О
| +1,23
| 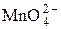 + 2H2O + 2 е =MnO2↓ + 4OH– + 2H2O + 2 е =MnO2↓ + 4OH–
| +0,58
|  +е = +е = 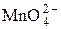
| +0,558
|  + 4H++3 е = MnO2↓ + 2H2O + 4H++3 е = MnO2↓ + 2H2O
| +1,69
|  + 2H2O + 3 e = MnO2↓ + 4OH– + 2H2O + 3 e = MnO2↓ + 4OH–
| +0,60
|  + 8H+ + 5 е = Mn2+ + 4H2O + 8H+ + 5 е = Mn2+ + 4H2O
| +1,51
| Продолжение табл. 14
|
|
|
| | Мо
| Мо3+ + 3 е = Mo↓
| –0,2
| 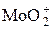 + 4H++2 e = Mo3+ + 2H2O + 4H++2 e = Mo3+ + 2H2O
| 0,0
| 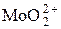 +e = +e = 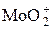
| +0,48
| | H2MoO4 + 6H+ + 6е = Mo↓ + 4H2O
| 0,0
| 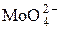 + 4Н2О + 6 е = Mo↓ + 8OH– + 4Н2О + 6 е = Mo↓ + 8OH–
| –1,05
| | N
| HN3 + 11H+ + 8 e = 3 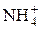
| +0,69
| | 3N2↑ + 2H+ + 2 е = 2HN3
| –3,1
| 3N2↑ + 2 е = 2 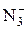
| –3,4
| | N2↑ + 2H2O + 4H+ + 2 е = 2(NH2OH·H+)
| –1,87
| | N2↑ + 4H2O + 2 е = 2NH2OH+ 2OH–
| –3,04
| | N2↑ + 5H+ + 4 е = N2H4·H+
| –0,23
| | N2↑ + 4H2O + 4 е = N2H4 + 4OH–
| –1,16
| N2↑ + 8H+ + 6 е = 2 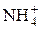
| +0,26
| | N2↑ + 8H2O + 6 е = 2NH4OH+ 6OH–
| –0,74
| N2H4·H+ + 3H+ + 2 е = 2 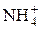
| +1,27
| | N2H4 + 4H2O + 2 е = 2NH4OH+ 2OH–
| +0,1
| NH2OH·H++2H+ + 2 е = 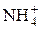 + H2O + H2O
| +1,35
| | NH2OH + 2H2O + 2 е = NH4OH + 2OH–
| +0,42
| | H2N2O2 + 2H+ + 2 е = N2↑ +2H2O
| +2,65
| | H2N2O2 + 6H+ + 4 е = 2(NH2OH·H+)
| +0,50
| | 2HNO2+ 4H+ + 4 e = H2N2O2 + 2H2O
| +0,83
| | HNO2 + H+ +е = NO↑ + H2O
| +0,98
|  + H2O + е = NO↑+ 2OH– + H2O + е = NO↑+ 2OH–
| –0,46
| | 2HNO2 + 4H+ + 4 e = N2O↑ + 3H2O
| +1,29
| | 2HNO2 + 6H+ + 4 e =N2↑ + 4H2O
| +1,44
| Продолжение табл. 14
|
|
|
| | N
| 2  + 4H2O + 6 е = N2↑ + 8OH– + 4H2O + 6 е = N2↑ + 8OH–
| +0,41
| HNO2 + 7H+ + 6 е = 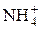 + 2H2O + 2H2O
| +0,86
|  + 6H2O + 6 е = NH4OH + 7OH– + 6H2O + 6 е = NH4OH + 7OH–
| –0,15
| | N2O↑ + 2H+ + 2 е = N2↑ + H2O
| +1,77
| | N2O↑ + H2O + 2 е = N2↑ + +2OH–
| +0,94
| | 2NO↑ +4H+ + 4 e = N2↑ + 2H2O
| +1,68
| | 2NO↑ +2H2O + 4 e = N2↑ + 4OH–
| +0,85
| | N2O4↑ + 2H+ + 2 е = 2HNO2
| +1,07
| N2O4↑ + 2 е = 2 
| +0,88
| | N2O4↑ + 8H++8е = N2↑ + 4H2O
| +1,35
| | N2O4↑ + 4H2O + 8 е = N2↑+8OH–
| +0,53
|  + 3H+ + 2 е = HNO2 + H2O + 3H+ + 2 е = HNO2 + H2O
| +0,94
|  + H2O + 2 е = + H2O + 2 е =  + 2OH– + 2OH–
| +0,01
|  + 2H+ + е = NO2↑ + H2O + 2H+ + е = NO2↑ + H2O
| +0,80
|  + H2O + e = NO2↑ +2OH– + H2O + e = NO2↑ +2OH–
| –0,86
|  + 4H+ + 3 е = NO↑ + 2H2O + 4H+ + 3 е = NO↑ + 2H2O
| +0,96
|  + 2H2O + 3 е = NO↑ + 4OH– + 2H2O + 3 е = NO↑ + 4OH–
| –0,14
| 2  + 12H+ + 10 e = N2↑+6H2O + 12H+ + 10 e = N2↑+6H2O
| +1,24
|  + 8H+ + 6 е = NH2OH·H+ + 2H2O + 8H+ + 6 е = NH2OH·H+ + 2H2O
| +0,73
| 2  + 17H++ 14 е = N2H4·H+ + 6H2O + 17H++ 14 е = N2H4·H+ + 6H2O
| +0,84
|  + 10H+ + 8 е = + 10H+ + 8 е = 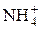 + 3H2O + 3H2O
| +0,87
|  + 7H2O + 8 е = NH4OH +9OH– + 7H2O + 8 е = NH4OH +9OH–
| –0,12
| | Na
| Na+ + e = Na↓
| –2,713
| | Nb
| Nb3+ + 3 е = Nb↓
| –1,1
| | Ni
| Ni2+ + 2 е = Ni↓
| –0,228
| Продолжение табл. 14
|
|
|
| | O
| O2↑ + 4H+ + 4 e = 2H2O
| + 1,229
| | O2↑ + 2H2O + 4 e = 4OH–
| +0,401
| | O2↑ + 2H+ + 2 е = H2O2
| +0,682
| O2↑ + H2O + 2е = 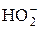 + OH– + OH–
| –0,076
| | H2O2 + 2H+ + 2 е = 2H2O
| +1,77
| 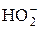 + H2O + 2 е = 3OH– + H2O + 2 е = 3OH–
| +0,88
| | O3↑ + 2H+ + 2 е = O2↑ + H2O
| +2,07
| | O3↑ + H2O + 2 е = O2↑ + 2OH–
| +0,02
| | Os
| Os2+ + 2 е = Os↓
| +0,85
| | OsO4↓ + 8H+ + 8 е = Os↓ + 4H2O
| +0,85
| | P
| P↓ + 3H+ + 3 e = PH3↑
| +0,06
| | P↓ + 3H2O + 3 e = PH3↑+3OH–
| –0,89
| | H3PO2 + H + + е = P↓ +2H2O
| –0,51
|  + е = P↓ + 2OH– + е = P↓ + 2OH–
| –2,05
| | H3PO3 + 3H+ + 3 е = P↓ + 3H2O
| –0,50
| | H3PO3+ 2H+ + 2 е = H3PO2 + H2O
| –0,50
|  + 2Н2O + 2 е = + 2Н2O + 2 е =  + 3OH– + 3OH–
| –1,57
| | H4P2O6 + 2H+ + 2 е = 2H3PO3
| +0,38
| | H3PO4 + 5H+ + 5 е = P↓+4H2O
| –0,41
| | H3PO4 + 4H+ + 4 е = H3PO2 + 2H2O
| –0,39
| | 2H3PO4 + 2H+ + 2 е = H4P2O6 + 2H2O
| –0,94
| | H3PO4 + 2H+ + 2 е = H3PO3 + H2O
| –0,276
| 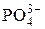 + 2H2O + 2 е = + 2H2O + 2 е =  + 3ОН– + 3ОН–
| –1,12
| | Рb
| Рb2+ + 2 е = Pb↓
| –0,126
| | Pb4+ + 2 е = Рb2+
| +1,66
| Продолжение табл. 14
|
|
|
| | Pb
| Pb4+ + 4 е = Pb↓
| +0,77
| | PbO2↓ + H2O + 2 е = PbO↓ + 2OН–
| +0,28
| | PbO2↓ + 4H+ + 2 е = Рb2+ + 2H2O
| +1,455
| | Pd
| Pd2+ + 2 е = Pd↓
| +0,915
| | Pt
| Pt2+ + 2е = Pt↓
| +1,2
| | S
| S↓ + 2 е = S2–
| –0,476
| | S↓ + 2H+ + 2 е = H2S↑
| +0,171
| | (SCN)2↑ + 2 е = 2SCN–
| +0,77
| 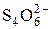 + 2 е = 2 + 2 е = 2 
| +0,09
|  + 6H+ + 4 e = 2S↓+3Н2О + 6H+ + 4 e = 2S↓+3Н2О
| +0,5
| 2Н2SО3 + 2Н+ + 4 e =  + 3H2O + 3H2O
| +0,40
| 2  + 3H2O + 4 e = + 3H2O + 4 e =  + 6OH– + 6OH–
| –0,58
| 2H2SO3+H+ + 2 е = 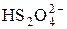 + 2Н2О + 2Н2О
| –0,08
| 2  + 2H2O + 2 е = + 2H2O + 2 е =  + 4OH– + 4OH–
| –1,12
|  + 4H+ + 2 е = H2SO3 + H2O + 4H+ + 2 е = H2SO3 + H2O
| +0,17
|  +H2O + 2 е = +H2O + 2 е =  + 2OH– + 2OH–
| –0,93
| 2  + 10H+ + 8 e = + 10H+ + 8 e =  + 5Н2О + 5Н2О
| +0,29
| 2  + 5H2O + 8 е = + 5H2O + 8 е =  + 10OH– + 10OH–
| –0,76
|  + 8H+ + 6 е = S↓ + 4H2O + 8H+ + 6 е = S↓ + 4H2O
| +0,36
|  + 4H2O + 6 е = S↓ + 8OH– + 4H2O + 6 е = S↓ + 8OH–
| –0,75
| 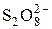 + 2 e = 2 + 2 e = 2 
| +2,01
| | Sb
| SbО+ + 2Н+ + 3 е = Sb↓+H2O
| +0,212
| | Sc
| Sc3+ + 3 е = Sc↓
| –2,08
| | Se
|  + H2O + 2 е = + H2O + 2 е = 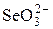 + 2OH– + 2OH–
| +0,05
| | Si
| 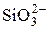 + 3H2O + 4 е = Si↓ + 6OH– + 3H2O + 4 е = Si↓ + 6OH–
| –1,7
| Продолжение табл. 14
|
|
|
| | Sn
| Sn2+ + 2 е = Sn↓
| –0,140
| | Sn4+ + 2 е = Sn2+
| +0,15
| | Sn4+ + 4е =Sn↓
| +0,01
| | Sr
| Sr2+ + 2 е = Sr↓
| –2,89
| | Te
| 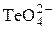 + H2O + 2 e = + H2O + 2 e =  + 2OH– + 2OH–
| +0,4
| | Th
| Th4+ + 4 е = Th↓
| –1,90
| | Ti
| Ti2+ + 2е = Тi↓
| –1,63
| | TiO2↓ + 4H+ + 4 е = Ti↓ + 2H2O
| –0,86
| | TiO2+ + 2H+ + 4 e = Ti↓ + H2O
| –0,88
| | TiO2+ + 2H+ + е = Ti3+ + H2O
| +0,1
| | Ti3+ + е = Ti2+
| –0,37
| | Tl
| Tl+ + е= Tl↓
| –0,357
| | Тl3+ + 2 е = Tl+
| +1,25
| | U
| U3+ + 3 е = U↓
| –1,80
| | U4+ + е = U3+
| –0,61
|  + 4H+ + 2 е =U4+ + 2H2O + 4H+ + 2 е =U4+ + 2H2O
| +0,33
| | V
| V2+ + 2 е = V↓
| –1,18
| | V3+ + е = V2+
| –0,255
| | VO2+ + 2H++ e =V3+ + H2O
| +0,337
| | VO2+ + e = VO+
| –0,044
| 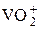 + 2H+ + е = VO2+ + H2O + 2H+ + е = VO2+ + H2O
| +1,000
| 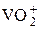 + 4H+ + 2 е = V3++ 2H2O + 4H+ + 2 е = V3++ 2H2O
| +0,668
| 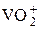 +4H+ + 3 е = V2++2H2O +4H+ + 3 е = V2++2H2O
| +0,360
| 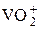 + 4H+ + 5 е = V↓ + 2H2O + 4H+ + 5 е = V↓ + 2H2O
| –0,25
|  + 6H+ + 2 е =VO+ + 3H2O + 6H+ + 2 е =VO+ + 3H2O
| +1,26
| Окончание табл. 14
|
|
|
| |
| 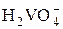 + 4H+ +е = VO2+ + 3H2O + 4H+ +е = VO2+ + 3H2O
| +1,31
| | W
| 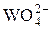 + 8H+ + 6 е = W↓ + 4H2O + 8H+ + 6 е = W↓ + 4H2O
| +0,05
| | Y
| Y3+ + 3 е = Y↓
| –2,37
| | Zn
| Zn2+ + 2 е = Zn↓
| –0,764
| | Zn(OH)2 + 2e = Zn↓ + 2OH–
| –1,245
| 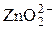 + 2H2O = Zn + 4OH– + 2H2O = Zn + 4OH–
| –1,216
| | Zr
| ZrO2↓ + 4H+ + 4 e = Zr↓ + 2H2O
| –1,43
|

Аальтернативная стоимость. Кривая производственных возможностей В экономике Буридании есть 100 ед. труда с производительностью 4 м ткани или 2 кг мяса...
|

Вычисление основной дактилоскопической формулы Вычислением основной дактоформулы обычно занимается следователь. Для этого все десять пальцев разбиваются на пять пар...
|

Расчетные и графические задания Равновесный объем - это объем, определяемый равенством спроса и предложения...
|

Кардиналистский и ординалистский подходы Кардиналистский (количественный подход) к анализу полезности основан на представлении о возможности измерения различных благ в условных единицах полезности...
|
|
Именные части речи, их общие и отличительные признаки Именные части речи в русском языке — это имя существительное, имя прилагательное, имя числительное, местоимение...
Интуитивное мышление Мышление — это психический процесс, обеспечивающий познание сущности предметов и явлений и самого субъекта...
Объект, субъект, предмет, цели и задачи управления персоналом Социальная система организации делится на две основные подсистемы: управляющую и управляемую...
|
|
Потенциометрия. Потенциометрическое определение рН растворов Потенциометрия - это электрохимический метод исследования и анализа веществ, основанный на зависимости равновесного электродного потенциала Е от активности (концентрации) определяемого вещества в исследуемом растворе...
Гальванического элемента При контакте двух любых фаз на границе их раздела возникает двойной электрический слой (ДЭС), состоящий из равных по величине, но противоположных по знаку электрических зарядов...
Сущность, виды и функции маркетинга персонала Перснал-маркетинг является новым понятием. В мировой практике маркетинга и управления персоналом он выделился в отдельное направление лишь в начале 90-х гг.XX века...
|
|